Винилхлорид — сырье для получения поливинилхлорида
Исходным сырьем для производства поливинилхлорида является винилхлорид.
Винилхлорид (хлористый винил) представляет собой при нормальных условиях бесцветный газ с температурой кипения —13,9 °С. Он хорошо растворяется в хлороформе, дихлорэтане, этаноле, эфире, ацетоне, углеводородах нефти и очень мало в воде. Наличие двойной связи обусловливает его способность к реакциям полимеризации.
Формула винилхлорида: CH2=CHCl
Получение винилхлорида
Винилхлорид может быть получен различными методами.
Гидрохлорирование ацетилена (рисунок 1 А) :
Процесс можно проводить в газовой и жидкой фазах в контактном аппарате трубчатого типа. Газофазный способ является наиболее распространенным. Процесс проводят в контактном аппарате трубчатого типа при 120— 220 °С под избыточным давлением 49 кПа над активированным углем, пропитанным хлоридом ртути в количестве 10% от массы угля.
Для газофазного гидрохлорирования применяется сухой 97—99%-ный ацетилен и высококонцентрированный хлористый водород в мольном соотношении 1 : 1,1. Хлористый водород не должен содержать свободного хлора, который с ацетиленом реагирует со взрывом.
Продукты реакции представляют собой газообразную смесь, которая содержит 93% винилхлорида и другие примеси. Эта смесь подвергается разделению и очистке.
Получение винилхлорида из этилена и хлора
Большое значение приобретают способы синтеза винилхлорида из этилена и хлора, так как этилен, получаемый из углеводородов нефти, является более дешевым, чем ацетилен, получаемый из карбида кальция или из природного метана и других углеводородов термоокислительным пиролизом или электрокрекингом.
Получение винилхлорида из этилена и хлора через дихлорэтан проводят в две стадии (рисунок 1 Б):
- жидкофазным хлорированием этилена в присутствии хлоридов меди, железа или сурьмы;
- пиролизом образовавшегося на первой стадии дихлорэтана.
Жидкофазное хлорирование этилена осуществляется в реакторе обычного типа при 45—60 °С в присутствии катализатора — хлорида железа в среде дихлорэтана. Полученный дихлорэтан подвергают пиролизу при 480—500 °С и давлении 0,15—0,20 МПа. В качестве катализатора применяется гранулированный активированный уголь или оксид алюминия, силикагель и железо.
Степень превращения достигает 70% за цикл. Дихлорэтан после его отделения направляется обратно в процесс.
Дегидрохлорирование дихлорэтана можно проводить над катализаторами, применяемыми при пиролизе дихлорэтана при 480—490 °С, под давлением 24 МПа в трубчатом реакторе из нержавеющей стали.
Разработан одностадийный способ получения винилхлорида высокотемпературным хлорированием этилена (рисунок 1 В):
Степень превращения этилена в винилхлорид возрастает с повышением температуры реакции хлорирования от 350 до 600,°С. При низких температурах наряду с замещением протекает реакция присоединения.
Высокотемпературное хлорирование этилена также можно проводить в присутствии винилхлорида в качестве разбавителя. Это позволяет увеличить концентрацию мономера в продуктах реакции [до 55% по объему], при этом затраты на выделение винилхлорида заметно снижаются.
Комбинированные методы получения винилхлорида
Основным недостатком методов получения винилхдорида из этилена и хлора является выделение хлористого водорода в качестве побочного продукта (550—650 кг на 1000 кг винилхлорида). Поэтому в настоящее время винилхлорид часто получают комбинированным методом (установки дегидрохлорирования дихлорэтана или установки хлорирования этилена комбинируют с установками гидрохлорирования ацетилена).
Проблема использования хлористого водорода, выделяющегося при дегидрохлорировании дихлорэтана, решается также совмещением установок получения и пиролиза дихлорэтана с установками окисления хлористого водорода, образующегося при пиролизе дихлорэтана. Процесс описывается уравнениями: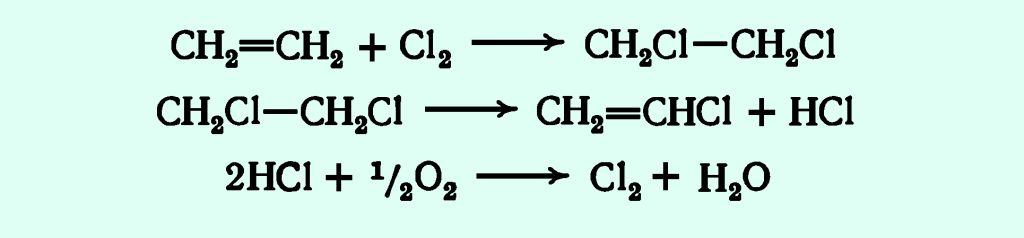
Образовавшийся хлор используется для хлорирования этилена. Вместо раздельного окисления хлористого водорода и хлорированного этилена до дихлорэтана можно применять одностадийный процесс окислительного хлорирования этилена: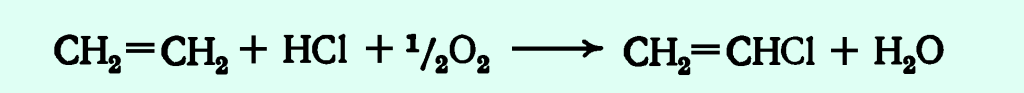
Реакция протекает над катализатором при 470—500 °С. В качестве катализатора применяют хлорид меди и хлорид калия на кизельгуре и другие.
Выход винилхлорида достигает 96% в пересчете на этилен и 90% в пересчете на хлористый водород.
В настоящее время разработаны технологические схемы, позволяющие использовать в производстве винилхлорида этилен и ацетилен без их предварительного выделения из разбавленных газов. На первой стадии происходит гидрохлорирование ацетилена, содержащегося в исходной смеси. Полученный винилхлорид экстрагируют дихлорэтаном, а оставшийся в смеси этилен подвергают хлорированию до дихлорэтана. Реакция протекает в среде дихлорэтана в присутствии хлорида железа под давлением 0,39—0,69. МПа.
Выделенный дихлорэтан перерабатывают в винилхлорид обычным путем, а образующийся хлористый водород используют для гидрохлорирования ацетилена.
Очистка и хранение винилхлорида
Получаемый различными методами винилхлорид необходимо подвергать тщательной очистке от ацетилена, хлористого водорода и других примесей.
Винилхлорид для получения поливинилхлорида должен содержать не менее 99,9% мономера и минимальное количество примесей. Чистый винилхлорид можно длительное время хранить в стальных цистернах при температурах от —50 до — 30 °С под азотом в отсутствие ингибиторов.
Читайте также:
- Винипласт (основная статья)
- Винипласт листовой (по ГОСТ 9639-71 в ред. 1990 г.) -маркировка и характеристики винипласта листового
- Поливинилхлорид (основная статья)
- Суспензионный поливинилхлорид
- Получение поливинилхлорида в массе
- Эмульсионный поливинилхлорид
- Пластикат ПВХ (мягкий ПВХ)
- Вспененный ПВХ
Коршак В. Б. Прогресс полимерной химии. М., Наука, 1965, 414 с.
Николаев А. Ф. Синтетические полимеры и пластические массы на их основе. Изд. 2-е. М. — Л., Химия, 1966. 768 с.
Николаев А. Ф. Технология пластических масс. Л., Химия, 1977. 367 с.
Кузнецов Е. В., Прохорова И. П., Файзулина Д. А. Альбом технологических схем производства полимеров и пластмасс на их основе. Изд. 2-е. М., Химия, 1976. 108 с.
Получение и свойства поливинилхлорид а/Под ред. Е. Н. Зильбермана. М., Химия, 1968. 432 с.
Лосев И. Я., Тростянская Е. Б. Химия синтетических полимеров. Изд. 3-е. М., Химия, 1971. 615 с.
Минскер К. С., Колесов С. В., Заиков Г. Е. Старение и стабилизация полимеров на основе винилхлорида. М., Химия, 1982. 272 с.
Хрулев М. В. Поливинилхлорид. М., Химия, 1964. 263 с.
Минскер /С. С, Федосеева Г. 7. Деструкция и стабилизация поливинилхлорида. М., Химия, 19 79.271 с.
Штаркман Б. Я. Пластификация поливинилхлорида. М., Химия, 1975. 248 с.
Фторполимеры/Пер. с англ. Под ред. И. Л. Кнунянца и Б. А. Пономаренко. М., Мир, 1975. 448 с.
Чегодаев Д. Д.., Наумова 3. К, Дунаевская Ц. С. Фторопласты. М.-Л. Госхимиздат, 1960. 190 с.
Автор: В.В. Коршак, академик
Источник: В.В. Коршак, Технология пластических масс,1985 год
Дата в источнике: 1985 год

