Поливинилхлорид (ПВХ)
Поливинилхлорид (ПВХ) [-СН2-СНСl-]n — это высокомолекулярный хлорсодержащий полимер, элементарные звенья в макромолекуле которого в основном соединены по типу «голова к хвосту».
Поливинилхлорид является термопластичным полимером с температурой стеклования 70—80 °С и температурой вязкого течения 150—200 °С в зависимости от молекулярной массы. Степень полимеризации ПВХ промышленных марок колеблется от 400 до 1500.
Свойства и назначение поливинилхлорида в значительной мере определяются способом его получения. Свойства ПВХ также можно изменять путем химической модификации. Доступность исходного сырья (винилхлорида), относительно несложные методы получения, ценные технические свойства обусловили быстрый рост и большие масштабы его производства.
Пластические массы на основе поливинилхлорида нашли широкое применение в электротехнической и химической промышленности, в строительстве, а также в других областях техники и в быту.
Краткий исторический очерк
В 1835 г. Реньо обнаружил способность газообразного винилхлорида под действием света превращаться в порошок. В 1872 г. полимеризация винилхлорида была исследована Бауманом. А через 40 лет Остромысленский и Клатте предложили использовать фотополимеризацию как промышленный метод получения поливинилхлорида. Позднее были разработаны способы полимеризации винилхлорида под влиянием инициаторов, распадающихся при нагревании на свободные радикалы. Промышленный синтез поливинилхлорида в водной эмульсии был впервые осуществлен в 1930 г. Следующим важным шагом явилась разработка и осуществление в промышленности суспензионной полимеризации винилхлорида. Сравнительно недавно был освоен промышленный метод полимеризации винилхлорида в массе.
Полимеризация винилхлорида
Поливинилхлорид (ПВХ) получают радикальной полимеризацией винилхлорида:
В промышленности наибольшее распространение получил суспензионный метод. Инициирование процесса осуществляется свободными радикалами, образующимися при гомолитическом распаде пероксидов или азосоединений. Первичный радикал присоединяется главным образом к метиленовой группе винилхлорида: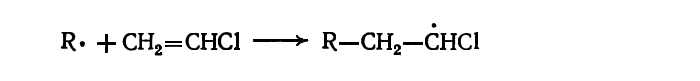
В связи со склонностью поливинилхлорида к дегидрохлорированию при температурах выше 75 °С возможна передача цепи на полимер за счет отрыва аллильного атома хлора от атома углерода, который находится рядом с двойной связью, образовавшейся вследствие частичного дегидрохлорирования полимера:
В результате этой реакции возникают малоактивные аллильные радикалы, вызывающие замедление полимеризации. Для предотвращения дегидрохлорирования и получения ПВХ с теоретическим содержанием хлора желательно вести процесс полимеризации при температурах не выше 70—75 °С.
Радикалы винилхлорида вследствие их высокой активности легко вступают во взаимодействие с различными примесями, содержащимися в мономере даже в незначительных количествах.
Некоторые из примесей, например ацетилен, реагируют как агенты передачи цепи и могут вызывать образование малоактивных радикалов, замедляя полимеризацию. В присутствии других примесей происходит обрыв цепи.
Реакция передачи цепи часто используется для регулирования молекулярной массы полимера. При этом в полимеризационную среду вводят вещества, способные участвовать в передаче цепи, — регуляторы. Регуляторы выбирают так, чтобы образующиеся в результате передачи цепи радикалы были достаточно активными, в противномслучае используемые регуляторы замедляют или даже ингибируют полимеризацию.
Во всех случаях получения поливинилхлорида кислород оказывает отрицательное влияние на ход полимеризации и свойства полимера. Наличие кислорода в системе обусловливает индукционный период процесса полимеризации, уменьшение скорости полимеризации, понижение средней молекулярной массы ПВХ, появление разветвленности, уменьшение термической стабильности ПВХ, ухудшение его совместимости с пластификаторами.
Поэтому содержание кислорода выше 0,0005—0,001% (по отношению к винилхлориду) нежелательно.
При полимеризации винилхлорида выделяется большое количество тепла 1466 кДж/кг, что существенно влияет на технологию получения полимера.
При полимеризации винилхлорида в массе полимер выпадает в осадок в виде твердой фазы вследствие нерастворимости ПВХ в мономере. При этом сначала происходит увеличение скорости реакции от начала процесса до высоких степеней конверсии мономера, а затем ее медленное уменьшение.
Возрастание скорости полимеризации обусловлено образованием твердой фазы. В результате передачи цепи на полимер на выпавших из жидкой фазы макромолекулах образуются активные центры, способные продолжать полимеризацию. Вследствие малой подвижности закрепленных на поверхности полимера растущих цепей скорость обрыва цепи уменьшается, тогда как скорость роста остается высокой из-за большой подвижности молекул мономера. Поэтому с появлением твердой фазы скорость полимеризации возрастает.
На возрастание скорости полимеризации винилхлорида влияет также способность полимера набухать в мономере. Полимеризация протекает в набухших частицах полимера, в которых скорость передвижения макрорадикалов, вероятность их столкновения и бимолекулярного обрыва цепи мала. Подвижность молекул мономера в набухших частицах и скорость роста полимерных цепей остается большой.
Описанное выше явление автокатализа при полимеризации винилхлорида в гетерогенных условиях часто называют гель-эффектом. Однако это явление при полимеризации винилхлорида не аналогично типичному гель-эффекту, наблюдаемому в тех случаях, когда образующийся полимер растворим в собственном мономере.
Свойства поливинилхлорида
 Поливинилхлорид представляет собой белый порошок плотностью 1350—1460 кг/м3. Молекулярная масса продукта промышленных марок 30000—150000. Степень кристалличности достигает 10%.
Поливинилхлорид представляет собой белый порошок плотностью 1350—1460 кг/м3. Молекулярная масса продукта промышленных марок 30000—150000. Степень кристалличности достигает 10%.
Поливинилхлорид характеризуется значительной полидисперсностью, возрастающей с увеличением степени превращения.
Среднечисловую молекулярную массу ‾Мn (близкую по значению к среднемассовой ¯Mw) можно рассчитать по значению характеристической вязкости [η]: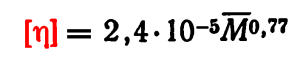
На практике молекулярную массу поливинилхлорида характеризуют константой Фикентчера (Кф): Kф=1000k
Коэффициент k определяется по уравнению :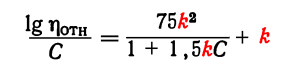
где ηотн — относительная вязкость раствора поливинилхлорида в циклогексаноне (обычно 0,5 или 1 г полимера на 100 см3 растворителя).
Ниже приводится константа Фикентчера Кф, характеризующая среднюю молекулярную массу поливинилхлорида, полученного различными способами:
| Способ получения ПВХ | Константа Фикентчера Кф |
| Суспензионный | 47-76 |
| В массе | 56-72 |
| Эмульсионный | 54 -77 |
Приведенная вязкость (ηпр), константа Фикентчера (Кф) и среднечисловая молекулярная масса (¯Мn) поливинилхлорида связаны следующим образом:
| ηпр | 1,80 | 1,98 | 2,20 | 2,44 | 2,70 |
| Кф | 55 | 60 | 65 | 70 | 75 |
| Мn | 50 000 | 65 000 | 80 000 | 90000 | 100 000 |
Благодаря высокому содержанию хлора (около 56%) поливинилхлорид не воспламеняется и практически не горит. При 130—150 °С начинается медленное, а при 170 °С более быстрое разложение поливинилхлорида, сопровождающееся выделением хлористого водорода.
Поливинилхлорид нерастворим в мономере (винилхлориде), в воде, спирте, бензине и многих других растворителях. При нагревании он растворяется в тетрагидрофуране, хлорированных углеводородах, ацетоне и др.
Поливинилхлорид обладает хорошими электроизоляционными и теплоизоляционными свойствами, а также высокой стойкостью к действию сильных и слабых кислот и щелочей, смазочных масел и др.
Под действием энергетических и механических воздействий в поливинилхлориде протекают реакции дегидрохлорирования, окисления, деструкции, структурирования, ароматизации и графитизации. Основная реакция, ответственная за потерю полимером эксплуатационных свойств, — выделение НСl.
Для предотвращения разложения в поливинилхлорид вводят стабилизаторы. В качестве антиоксидантов применяют производные фенолов и производные карбамида.
При термической пластификации при 160 °С поливинилхлорид превращается в застывший блок, жесткий и прочный при комнатной температуре.
Поливинилхлорид хорошо совмещается с пластификаторами.
Поливинилхлорид широко используется в технике как антикоррозионный материал. Благодаря хорошим электроизоляционным свойствам он применяется для кабельной изоляции и для других целей.
Читайте также:
- Суспензионный поливинилхлорид
- Получение поливинилхлорида в массе
- Эмульсионный поливинилхлорид
- Винилхлорид — сырье для получения поливинилхлорида
Дополнительную информацию по теме поливинилхлорида (новости, аналитика, прогнозы, литература и прочее) на портале MPlast.by вы можете найти на странице темы — ПВХ.
Коршак В. Б. Прогресс полимерной химии. М., Наука, 1965, 414 с.
Николаев А. Ф. Синтетические полимеры и пластические массы на их основе. Изд. 2-е. М. — Л., Химия, 1966. 768 с.
Николаев А. Ф. Технология пластических масс. Л., Химия, 1977. 367 с.
Кузнецов Е. В., Прохорова И. П., Файзулина Д. А. Альбом технологических схем производства полимеров и пластмасс на их основе. Изд. 2-е. М., Химия, 1976. 108 с.
Получение и свойства поливинилх лор ид а/Под ред. Е. Н. Зильбермана. М., Химия, 1968. 432 с.
Лосев И. Я., Тростянская Е. Б. Химия синтетических полимеров. Изд. 3-е. М., Химия, 1971. 615 с.
Минскер К. С., Колесов С. В., Заиков Г. Е. Старение и стабилизация полимеров на основе винилхлорида. М., Химия, 1982. 272 с.
Хрулев М. В. Поливинилхлорид. М., Химия, 1964. 263 с.
Минскер /С. С, Федосеева Г. 7. Деструкция и стабилизация поливинилхлорида. М., Химия, 1979. 271 с.
Штаркман Б. Я. Пластификация поливинилхлорида. М., Химия, 1975. 248 с.
Фторполимеры/Пер. с англ. Под ред. И. Л.Кнунянца и Б. А. Пономаренко. М., Мир, 1975. 448 с.
Чегодаев Д. Д.., Наумова 3. К, Дунаевская Ц. С. Фторопласты. М.-Л.,Госхимиздат, 1960. 190 с.
Автор: Коршак В.В.
Источник: Коршак В.В, Технологии пластических масс, 3-е издание, 1985 год
Дата в источнике: 1985 год
