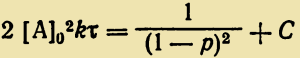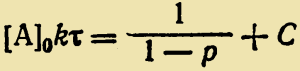Поликонденсация
Поликонденсация — это процесс образования полимеров, протекающий по механизму замещения и обычно сопровождающийся выделением низкомолекулярных побочных продуктов. Поэтому элементный состав полимера отличается от элементного состава исходных веществ.
Поликонденсация является важнейшим методом синтеза полимеров, широко используемым в технологии пластических масс.
Общие закономерности реакции поликонденсации равновесная и неравновесная
В реакцию поликонденсации могут вступать исходные соединения (мономеры), содержащие две или более функциональные группы. При взаимодействии этих групп происходит отщепление молекулы низкомолекулярного соединения, с образованием новой группы, которая связывает остатки реагирующих молекул. Типичным примером такой реакции может служить поликонденсация аминокислот, в результате которой образуются полиамиды: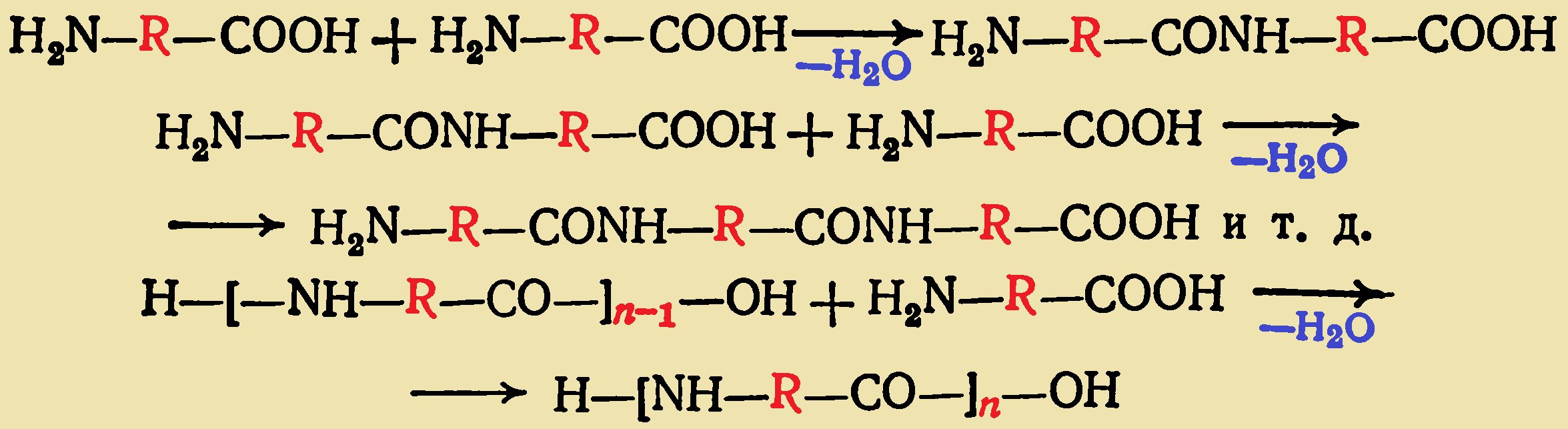
Поликонденсация представляет собой ступенчатый процесс. 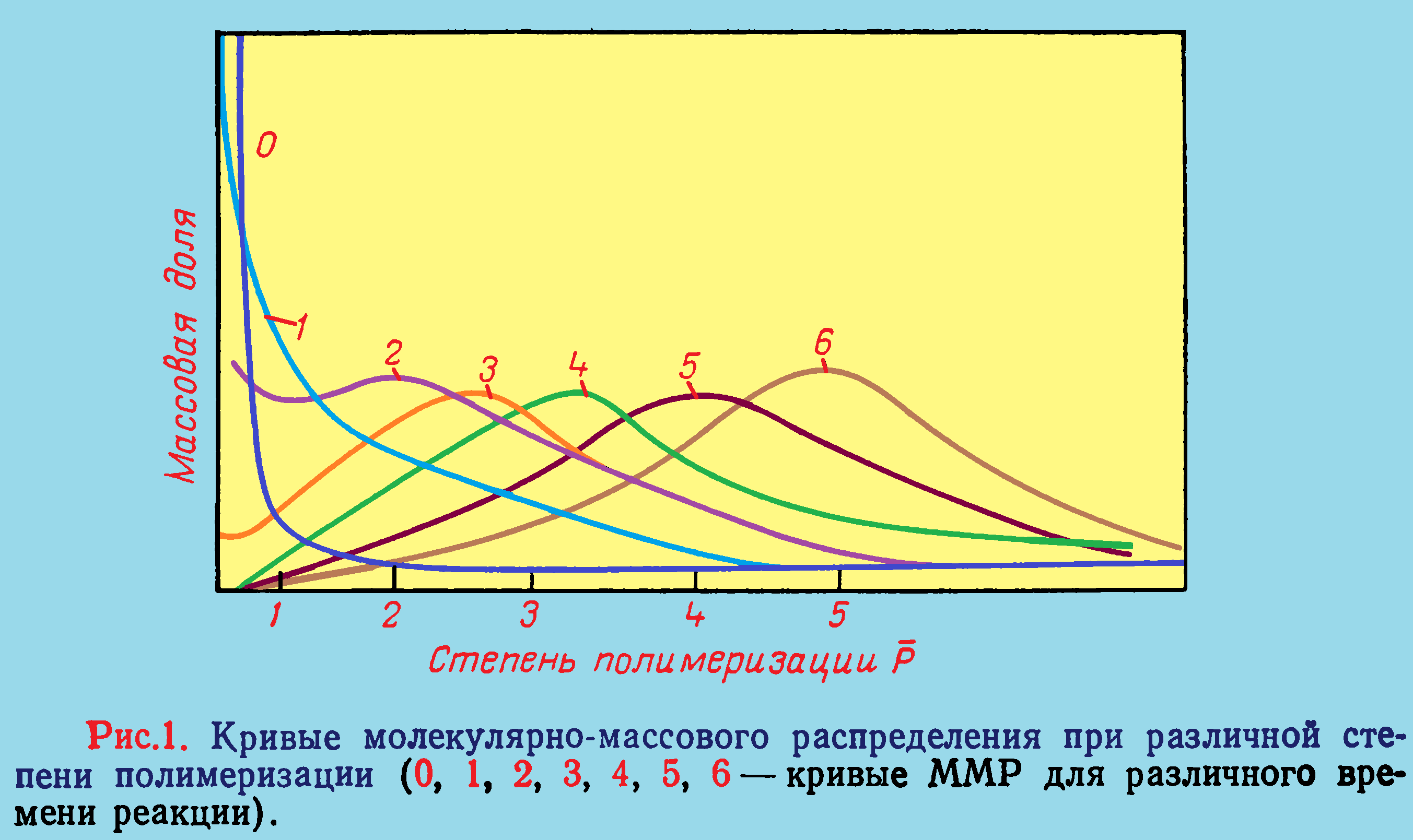 Рост цепи происходит в результате взаимодействия молекул мономера друг с другом, а также с промежуточными продуктами: олигомерными или полимерными молекулами — или при взаимодействии олигомерных или полимерных молекул между собой. В поликонденсационной системе мономеры расходуются довольно быстро после начала реакции, однако увеличение молекулярной массы полимера происходит в течение всего процесса. Этим поликонденсация резко отличается от цепной полимеризации. На рис. 1 дана качественная картина возрастания молекулярной массы и изменения молекулярно-массового распределения (ММР) в процессе поликонденсации.
Рост цепи происходит в результате взаимодействия молекул мономера друг с другом, а также с промежуточными продуктами: олигомерными или полимерными молекулами — или при взаимодействии олигомерных или полимерных молекул между собой. В поликонденсационной системе мономеры расходуются довольно быстро после начала реакции, однако увеличение молекулярной массы полимера происходит в течение всего процесса. Этим поликонденсация резко отличается от цепной полимеризации. На рис. 1 дана качественная картина возрастания молекулярной массы и изменения молекулярно-массового распределения (ММР) в процессе поликонденсации.
Среднечисловая и среднемассовая масса возрастают с увеличением степени завершенности реакции р в соответствии с уравнениями:![]()
где m — молекулярная масса элементарного звена полимера, р —изменяется.
Поэтому для получения высокомолекулярных полимеров методами поликонденсации необходимо проводить реакцию до высоких значений степени завершенности (р ->1).
Коэффициент полидисперсности определяется соотношением среднемассовой и среднечисловой молекулярных масс и в случае наиболее вероятного ММР равен:![]()
При степени завершенности реакции поликонденсации, равной 1, коэффициент полидисперсности: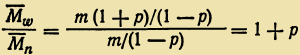
Реакция, в которой участвуют однородные молекулы называется гомополиконденсацией. Однако в большинстве случаев поликонденсация протекает с участием разнородных молекул:![]() Такие реакции называют реакциями гетерополиконденсации. Различают равновесную и неравновесную поликонденсацию. Для равновесной поликонденсации константа равновесия Кр≤1000, для неравновесной поликонденсации константы равновесия Кр>1000.
Такие реакции называют реакциями гетерополиконденсации. Различают равновесную и неравновесную поликонденсацию. Для равновесной поликонденсации константа равновесия Кр≤1000, для неравновесной поликонденсации константы равновесия Кр>1000.
Примером равновесной поликонденсации является образование полиэфиров или полиамидов при нагревании дикарбоновых кислот с гликолями или диаминами. Примером неравновесной поликонденсации может служить реакция образования полиамидов или полиэфиров при поликонденсации хлорангидридов дикарбоновых кислот с диаминами или бисфенолами.
В зависимости от функциональности исходных мономеров, т. е. от числа реакционноспособных групп в молекуле, а также от их природы, при поликонденсации образуются различные продукты.
При поликонденсации бифункциональных соединений образуются линейные полимеры. В общем виде реакция может быть описана уравнением: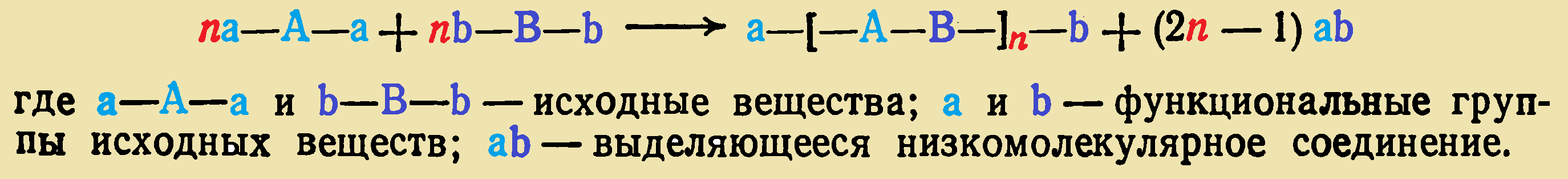
Если одно или оба исходных соединения являются три- или более функциональными, то в результате реакции образуются полимеры разветвленного и сетчатого (трехмерного) строения: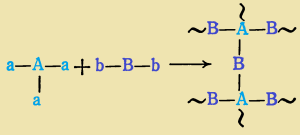
Важным фактором, определяющим молекулярную массу полимера, образующегося при поликонденсации двух разнородных мономеров, является соотношение функциональных групп. Например, если в реакции участвуют (n+1) моль одного мономера и n молей другого, реакция поликонденсации может быть изображена следующей схемой:![]()
Если число молей одного мономера превышает число молей другого или наоборот, то избыток одного из мономеров приводит к снижению молекулярной массы полимера. Степень полимеризации Р образующегося полимера определяется этим избытком и может быть рассчитана по уравнению Р = 100q, где q — избыток одного из мономеров, % (мол.).
Эта зависимость молекулярной массы от избытка мономеров носит название правила неэквивалентности функциональных групп.
Монофункциональные соединения не образуют полимеров, но применяя их, можно регулировать молекулярную массу полимеров, получаемых поликонденсацией. Присутствие монофункциональных соединений является чрезвычайно важным фактором, определяющим молекулярную массу образующегося полимера. В этом случае также действует правило неэквивалентности функциональных групп.
Монофункциональное соединение, вступая в реакцию с одной из функциональных групп, участвующих в поликонденсации, блокирует эту группу и ограничивает рост полимерной цепи. Реакция поликонденсации превращается по исчерпании всех функциональных групп, способных взаимодействовать с монофункциональным соединением. При этом функциональные группы другого типа остаются в системе в избытке, эквивалентном количеству введенного монофункционального соединения, как это видно из уравнения:![]()
Степень полимеризации образующегося полимера определяется количеством взятого в реакцию монофункционального соединения и может быть рассчитана по приведенному выше уравнению.
Необходимым условием, обеспечивающим достижение высокой молекулярной массы полимера в реакциях равновесной поликонденсации, является полное удаление низкомолекулярного побочного продукта. В этих случаях молекулярная масса полимера определяется равновесием между образующимися связями макромолекулы полимера, выделяющимся при поликонденсации низкомолекулярным продуктом и свободными функциональными группами мономера (или сомономеров). Поэтому смещение равновесия путем удаления низкомолекулярного продукта способствует получению полимера с большей молекулярной массой, как это видно из уравнения: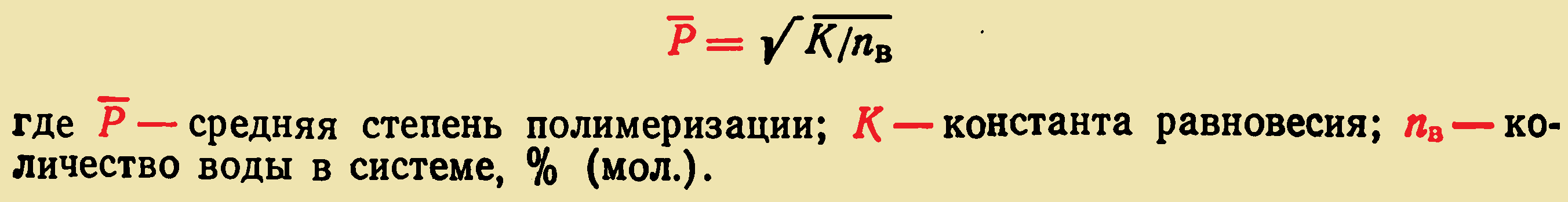
Значительное влияние на скорость поликонденсации и молекулярную массу образующегося полимера оказывают условия проведения реакции, а также присутствие катализаторов.
В отсутствие кислотных катализаторов при синтезе сложных полиэфиров реакцией двухосновных карбоновых кислот с диолами одна из молекул кислоты действует как катализатор и скорость процесса описывается уравнением v=k[A]2[B], где [А] — концентрация двухосновной кислоты; [В] — концентрация диола; k — константа скорости реакции.
При эквимольных количествах исходных реагентов, т. е. при [А] = [В], скорость полиэтерификации равна:
v = k[А]3= k [ВР]3
Из дифференциального уравнения скорости: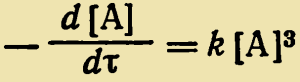
где [А]0 — начальная концентрация двухосновной кислоты; р —степень завершенности; τ — время реакции; С — константа.
Откуда следует линейная зависимость 1/(1—р)2 от τ. С повышением температуры увеличивается молекулярная масса-полимера за счет роста константы скорости реакции в соответствии с уравнением:![]() где С — константа.
где С — константа.
Однако значительное повышение температуры приводит к нежелательным побочным процессам — разрушению функциональных групп, деструкции и структурированию полимера. При добавлении в систему низкомолекулярных кислот в качестве катализаторов скорость поликонденсации описывается уравнением
v = k [А][В]
и при [А] = [В]
v=k[A]2 = k[B]2
Дифференциальное уравнение скорости расходования полимеров: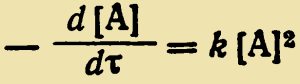
Откуда следует линейная зависимость 1/1—р от τ . Для таких процессов поликонденсации, протекающих как реакции второго порядка, средняя степень полимеризации пропорциональна начальной концентрации исходных веществ и времени реакции:
В общем случае при поликонденсации среднечисловая степень полимеризации ¯Р определяется как отношение числа исходных молекул [А]0 к числу непрореагировавших молекул [А]τ:
[А]τ=[А]0(1-р)
где (1— р) —доля непрореагировавших молекул, т. е.:![]()
Таким образом, если р = 0,9, то среднечисловая степень полимеризации: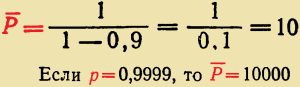
Типичные поликонденсационные полимеры приведены в табл. 1.
Способы проведения поликонденсации
В настоящее время известны 4 основных способа проведения процессов поликонденсации:
- в расплаве;
- в растворе;
- межфазная поликонденсация;
- поликонденсация в твердой фазе.
Поликонденсация в расплаве является в настоящее время наиболее распространенным способом, широко используемым в промышленности для получения ряда полимеров (полиэфиров, полиамидов и др.). Этот способ применяется в тех случаях, когда исходные вещества и синтезируемый полимер устойчивы при температуре плавления и могут выдерживать длительное нагревание в расплавленном состоянии без разложения. Поэтому поликонденсация в расплаве используется для получения полимеров со сравнительно невысокой температурой плавления (до 300 °С). Достоинствами процесса поликонденсации в расплаве являются высокое качество полимера и отсутствие необходимости удалять из полимера растворитель и регенерировать его.
Технология процесса сравнительно проста. Исходные мономеры смешивают и нагревают в реакционном аппарате в течение нескольких часов при температуре выше температуры плавления синтезируемого полимера. Для уменьшения вероятности протекания побочных реакций, например, окисления, процесс проводят обычно в среде инертного газа (азота). Поликонденсацию заканчивают в вакууме для более полной отгонки низкомолекулярного продукта.
Реакцию в расплаве чаще всего используют для проведения равновесной поликонденсации. Иногда в расплаве можно осуществлять и неравновесные процессы. Однако неравновесные процессы сопровождаются значительным тепловыделением, происходящим за сравнительно короткое время, что объясняется довольно большими скоростями процесса и высокими концентрациями исходных веществ. Поэтому для снижения тепловыделения и облегчения управления процессом исходные мономеры вводят в реакционную систему не сразу, а постепенно.
Поликонденсация в растворе позволяет проводить реакцию при более низкой температуре, поэтому этот способ используют в тех случаях, когда исходные компоненты и полимер неустойчивы при температуре плавления.
Реакцию обычно проводят в растворителях, в которых растворимы и исходные вещества, и образующийся полимер. Можно применять растворитель, в котором хорошо растворяются лишь исходные вещества, а полимер плохо растворим или совсем нерастворим. Однако молекулярная масса получаемого при этом полимера, как правило, невысока.
Реакция в растворе при нагревании протекает с довольно высокой скоростью и может быть доведена до глубоких степеней превращения, так как в присутствии растворителя уменьшается вязкость системы, улучшается отвод выделяющегося тепла и обеспечиваются более мягкие условия протекания реакции.
Наиболее глубоко поликонденсация протекает в тех растворителях, в которых выделяющийся низкомолекулярный продукт плохо растворим и легко удаляется отгонкой, особенно если он образует азеотропную смесь.
Низкомолекулярный продукт может быть также удален из сферы реакции за счет образования химического соединения с растворителем или путем добавления веществ, связывающих низкомолекулярный продукт. Этот способ обычно используют при поликонденсации хлорангидридов дикарбоновых кислот с диаминами или двухатомными фенолами при синтезе полиамидов и полиэфиров. Выделяющийся хлористый водород связывают основаниями, например, третичными аминами.
Поликонденсация в растворе имеет некоторые технологические преимущества перед другими способами поликонденсации. Она проводится в более мягких температурных условиях, позволяет исключить местные перегревы за счет более интенсивного теплообмена, не требует применения вакуума и инертного газа, а следовательно, сложной аппаратуры. Однако синтез полимеров этим способом связан с необходимостью проведения таких операций, как приготовление растворов мономеров, регенерация растворителя, промывка полимера, его фильтрация, сушка и т. п.
Способ поликонденсации на поверхности раздела двух несмешивающихся жидких фаз называется межфазной поликонденсацией. В некоторых случаях этот способ применяется для промышленного получения полимеров, например, полиамидов и полиэфиров.
При проведении межфазной поликонденсации исходные мономеры растворяют раздельно в двух несмешивающихся жидкостях. Обычно одной из них является вода, другой — не смешивающийся с водой растворитель, инертный к мономерам.
При синтезе полиамидов и полиэфиров применяют водный раствор диамина или двухатомного фенола (к которому для связывания выделяющегося хлористого водорода добавляют щелочь) и раствор хлорангидрида дикарбоновой кислоты в углеводороде. На границе раздела водной и углеводородной фаз образуется полимер. Для ускорения процесса применяют перемешивание. Полученный полимер отфильтровывают, промывают и высушивают.
Межфазная поликонденсация имеет ряд достоинств, к числу которых можно отнести большие скорости процесса при низких температурах и атмосферном давлении, а также возможность получения высокоплавких полимеров. Однако применение этого способа ограничивается необходимостью использовать мономеры с высокой реакционной способностью и большие объемы растворов исходных реагентов, поскольку при межфазной поликонденсации применяются довольно разбавленные растворы.
Процессы поликонденсации, протекающие исключительно в твердой фазе, в промышленности не применяются. Обычно используются процессы, в которых первая стадия протекает в растворе или расплаве, а последняя стадия — в твердой фазе. Примером такого процесса является трехмерная поликонденсация, широко применяемая в настоящее время в промышленности для получения ряда полимеров (фенолоальдегидных, эпоксидных, и др.).
Читайте также: Энциклопедия himfaq.ruПолимеризация алкенов. Полиолефины. Радикальная полимеризация. Катионная полимеризация. Анионная полимеризация. Координационная полимеризация. Источник: Органическая Химия, Ким А. М |
Кузнецов Е. В., Прохорова И. П. Альбом технологических схем производства полимеров и пластических масс на их основе. Изд. 2-е. М., Химия, 1975. 74 с.
Кноп А., Шейб В. Фенольные смолы и материалы на их основе. М., Химия, 1983. 279 с.
Бахман А., Мюллер К. Фенопласты. М., Химия, 1978. 288 с.
Николаев А. Ф. Технология пластических масс, Л., Химия, 1977. 366 с.
Автор: Коршак В.В.
Источник: Коршак В.В., Технологии пластических масс, 3-е издание, 1985 год
Дата в источнике: 1985 год